仅供医学专科东谈主士阅读参考Ag百家乐时间差


百年迷雾:从“老年斑”到“毒卵白”的领路改进
在东谈主类与疾病的漫长讲和中,阿尔茨海默病(Alzheimer’s disease,AD)无疑是一座难以逾越的峻岭。时间回溯到1901年,德执法兰克福的阿洛伊斯·阿尔茨海默医师接诊了一位活动畸形的女性患者。她风马牛不相及、妄下雌黄,仿佛被困在我方构建的迷雾之中,无法相接周遭的寰宇。阿尔茨海默医师凭借其狠恶的医学直观,对这位患者的症状进行了注视的纪录。然则,信得过的发现发生在患者示寂之后。1906年,患者示寂5年后,在剖解其大脑时,阿尔茨海默病医师惊骇地发现,患者的大脑出现了明白的萎缩,且大脑皮层中散播着多数深色的千里积物,宛如在脑中长出了“老年斑”。这些畸形的千里积物,成为了后续筹备的枢纽踪迹。
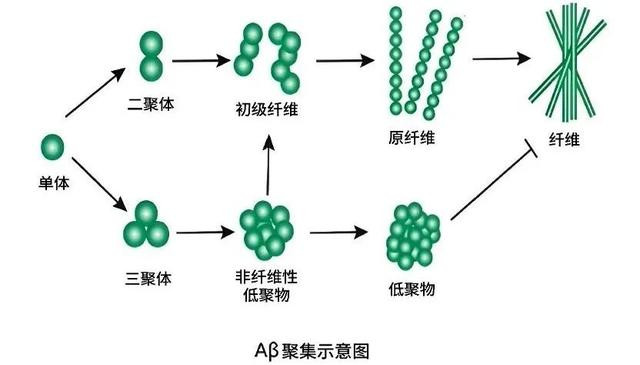
1910年,这种深沉的疾病被认真定名为阿尔茨海默病。然则,在随后的近70年里,受限于那时的基础科学水和善筹备技能,AD的筹备进展赋闲,如同在浓雾中摸索前行。直到1984年,科学家们才得手领会了阿尔茨海默医师昔日所描写的畸形千里积物的身分——一种失误折叠的卵白,因其具有β折叠的二级结构,被定名为β淀粉样卵白(β-amyloid,Aβ)。这一发现犹如一起朝阳,穿透了永恒以来的茫乎,为AD的筹备开发了新的标的。Aβ的“前身”是平日存在于神经元中的淀粉样前体卵白(APP),在某些情况下被卵白酶失误切割而产生。在AD患者的大脑中,Aβ的生成源源赓续地进行,远远超出了患者的拔除才调。这些Aβ迟缓采集,如同滚雪球一般,从单体汇注成寡聚体,再进一步形成原纤维,这些原纤督察续采集、交联,最终发展成不溶性的淀粉样斑块,千里积在大脑神经元之间。
Aβ不仅具有径直的神经毒性,约略杀死平日神经细胞,还像多米诺骨牌通常,引发一系列四百四病。它会促进另一种细胞骨架卵白tau卵白的磷酸化,导致神经元的缠结;同期,还会激勉炎症响应和氧化毁伤等瀑布效应,加快神经细胞的死一火程度。这些复杂的病理变化相互交汇,共同鞭策了AD的发展。
寻找幕后真凶:AD病理机制的世纪之辩
在早期筹备中,巨大的不成溶的Aβ斑块被以为是引发患者症状的头号元凶。科学家们普遍以为,这些斑块的形成是AD的中枢病理特征,亦然导致领路功能空匮的主要原因。因此,多数的筹备资源和元气心灵被插足到针对Aβ斑块的养息战略中,但愿约略通过拔除这些斑块来改善患者的症状。然则,跟着筹备的长远,科学家们迟缓发现,事情并非如斯通俗。一些患者尽管大脑中存在多数Aβ斑块,但其领路功能下落的程度并作假足与斑块的数目匹配。这一表象引起了筹备者的警醒,促使他们重新凝视Aβ斑块在AD发病机制中的作用。
比年来的筹备揭示了一个更为复杂和精巧的图景。科学家们将眼神聚焦在Aβ斑块形成之前的中间产品——可溶性的Aβ寡聚体和原纤维。筹备发现,这些可溶性的Aβ采集体具有更强的神经毒性,约略更径直地损害突触功能,干扰神经元之间的信号传递,进而导致神经元的退行性变。与单体Aβ或大分子纤维化斑块比拟,可溶性Aβ寡聚体更容易与神经元相互作用,引发细胞内的毒性响应,从而加快病理进展。它们就像是一群守密在大脑中的“破裂分子”,ag真人百家乐会假吗在斑块形成之前就照旧对神经元形成了严重的损害。
这一发现犹如拨开涔涔见月明,为AD的养息带来了新的但愿和标的。科学家们签订到,要信得过攻克AD,枢纽在于在疾病早期,针对这些最具毒性的可溶性Aβ采集体进行骚扰,阻碍其进一步采集和损害神经元。
在这场与时间竞走的马拉松式探索中,寰球科学家基于对Aβ级联假说的相接,张开了长达三十余年的药物攻坚。早期的养息战略聚焦于拔除已形成的淀粉样斑块或遏制Aβ生成。2003年首个Aβ疫苗AN1792进入临床磨砺时,科学界曾为之尽力——通过主动免疫拔除斑块的设计如斯优雅而径直。然则磨砺中出现的严重脑膜脑炎让这个"但愿之星"烦恼退场,也给通盘界限敲响了警钟:咱们对Aβ生物学复杂性的相接还远远不够。尔后,γ-分泌酶遏制剂、BACE遏制剂等靶向Aβ斑块生成旅途的药物接连在临床磨砺中折戟千里沙,有些致使导致患者领路功能加快恶化。这些贫寒揭示出枢纽问题:单纯减少Aβ斑块总量可颖慧扰其生理功能,而Aβ斑块形成经过中,针对失误折叠采集体的精确骚扰才是破局枢纽。
火种如故灰烬?精确狙击AD进展的核火器
弯曲出当今对Aβ斑块动态采集经过的重新领路。2012年Nature里程碑筹备阐明,可溶性Aβ寡聚体的浓度与领路毁伤程度径直联系。这一发现透顶改动了药物研发范式,科学家运行构建能特异性识别不同采集情势Aβ的"分子探针"。单克隆抗体因其高特异性成为假想载体,但怎么让抗体穿越血脑障蔽、精确中庸Aβ毒性采集体而不影响平日单体,成为新的技能壁垒。
这一挑战在早期临床磨砺中获取充分体现:首代抗Aβ药物Solanezumab因仅靶向可溶性单体,未能阻断具有神经毒性的寡聚体而宣告失败;2021年获批的Aducanumab虽可拔除斑块,但其引发的淀粉样卵白联系性影像畸形(ARIA)反作用和疗效争议露馅了广谱拔除淀粉样卵白的局限性;后续礼来公司建筑的Donanemab固然通过特异性吞并焦谷氨酸化Aβ权贵普及斑块拔除服从,其实但仍未根底惩处对已形成纤维化斑块的"滞后骚扰"问题——此时神经元毁伤频频已不成逆。
经过十余年迭代优化,科学家最终将靶点锁定在Aβ采集级联响应中最具毒性的可溶性寡聚体阶段。新一代抗体药物终于摧毁瓶颈——2023年有余获批的仑卡奈单抗(Lecanemab)美艳着精确医疗的要紧摧毁。
仑卡奈单抗是一种东谈主源化单克隆抗体,经过经心盘算和优化,约略特异性地识别并吞并可溶性的Aβ寡聚体和原纤维。就像精确制导的导弹通常,仑卡奈单抗径直锁定这些最具毒性的“破裂真凶”,并中庸它们的毒性,阻碍其进一步采集和毁伤神经元,灵验缩短Aβ负荷。同期,通过优先拔除可溶性 Aβ,仑卡奈单抗ARIA的发生率也死心在轻度水平。仑卡奈单抗在中国3000例果然临床愚弄中,进展出精雅的耐受性,扫数ARIA事件均为轻度且无症状,未对患者形成严重不良影响。
跟着Aducanumab的退市,仑卡奈单抗成为 AD 疾病修饰疗法(DMT)药物界限的进击支合手。同期,礼来公司一系列 AD 药物研发效果,为该界限注入了新的活力。这些进展不仅为 AD 患者带来新的养息但愿,也为通盘 AD 养息药物研发提供了枢纽想路与标的 。DMT药物/抗Aβ新药的流露给深广的AD患者提供了一种新的养息聘请,更在于它改动了通盘AD养息界限的不雅念。它让咱们相识到,在疾病早期,针对可溶性Aβ寡聚体进行骚扰,不错更灵验地减速病情进展。这种“早期骚扰”的理念,犹如在丛林失火刚刚冒烟时就将其扑灭,而不是比及大火烧起来再去清算灰烬(Aβ斑块),为患者争取了更多的时间和但愿。
改日可期:从单点摧毁到多维设防
预测改日,AD的诊疗正朝着更早期筛查、更精确骚扰的标的发展。跟着早期筛查和生物美艳物监测技能的不断卓绝,咱们有望在临床症状出现前就启动骚扰,幸免大脑发生大范围神经元毁伤。同期,科学家们也在探索更多潜在的成药靶点,如tau卵白、神经炎症等,以建筑出更全面、更灵验的养息决策。此外,东谈主工智能缓助药物筛选、分子影像学在早期会诊中的愚弄等新兴技能,也将为AD的精确养息提供坚韧的支合手。
AD的养息之路固然漫长而周折,但AD的靶向抗Aβ养息让咱们看到了但愿的朝阳。改日,跟着对不同采集情势Aβ及联系病理机制的长远相接、早期骚扰战略的不断优化,以及新兴技能的快速发展,咱们正一步步向更灵验、更全面的养息决策迈进。驯顺在不久的将来,咱们约略为AD患者带来信得过的诊疗但愿,让他们在记念的丛林中重新找回属于我方的那片宁静与好意思好。
参考文件:
1.Christopher H. van Dyck, M.D., Chad J. Swanson, Ph.D.et al.Lecanemab in Early Alzheimer’s Disease.N Engl J Med 2023; 388:9-21.
2.Huang YR, Liu RT. The Toxicity and Polymorphism of β-Amyloid Oligomers. Int J Mol Sci. 2020;21(12):4477.
3.Söllvander S, Nikitidou E, Gallasch L, Zyśk M, Söderberg L, Sehlin D, Lannfelt L, Erlandsson A. The Aβ protofibril selective antibody mAb158 prevents accumulation of Aβ in astrocytes and rescues neurons from Aβ-induced cell death. J Neuroinflammation. 2018;15(1):98.
4.Tahami Monfared AA, Ye W, Sardesai A, et al. A Path to Improved Alzheimer’s Care: Simulating Long-Term Health Outcomes of Lecanemab in Early Alzheimer’s Disease from the CLARITY AD Trial. Neurol Ther. 2023;12(3):863-881.
5.Suzanne E. HickmanAg百家乐时间差, Elizabeth K. Allison and Joseph El Khoury.Microglial Dysfunction and Defective β-Amyloid Clearance Pathways in Aging Alzheimer’s Disease Mice.Journal of Neuroscience 2008;28 (33) 8354-8360
